Етилацетат
Шаблон:Речовина Ети́лацета́т — органічна сполука ряду естерів. Має хімічний склад CH3COOC2H5 і умовно розглядається як продукт взаємодії етанолу та оцтової кислоти. За звичайних умов є безбарвною рідиною з приємним, фруктовим запахом. Добре розчиняється у воді, необмежено змішується з етанолом.
Широко застосовується як розчинник у виробництв покриттів, адгезивів, лікарських засобів, а також як екстрагент у харчовій промисловості.
Фізичні властивості

Етилацетат є безбарвною рідиною із фруктовим запахом. Він утворює азеотропну суміш з водою, яка кипить при 70,38 °C і містить 8,47% води та 91,53% естеру. Виділення етилацетату з водно-етанольного розчину відбувається у вигляді азеотропної суміші естер-спирт-вода, яка кипить за 70,2 °C і містить 9,0% води, 8,4% етанолу і 82,6% естеру.
| 0 °C | 10 °C | 20 °C | 30 °C | 40 °C | 50 °C | 60 °C | 70 °C | 80 °C | 90 °C | 100 °C |
|---|---|---|---|---|---|---|---|---|---|---|
| 0,9245 | 0,9126 | 0,9006 | 0,8884 | 0,8759 | 0,8632 | 0,8503 | 0,8370 | 0,8234 | 0,8095 | 0,7952 |
| 0 °C | 25 °C | 50 °C | 75 °C |
|---|---|---|---|
| 0,578 | 0,423 | 0,325 | 0,259 |
Отримання
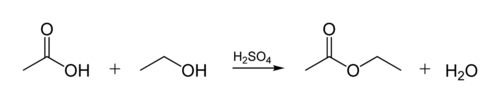
Основним застосовуваним методом для синтезу етилацетату є взаємодія оцтової кислоти та етанолу (естерифікація):
Виділення естеру з реакційної суміші відбувається у вигляді азеотропної суміші естер-спирт-вода. Після декантації та очищення кінцевий вихід продукту складає 95%.
Оцтова кислота є порівняно слабким ацилюючим агентом, тому для збільшення ефективності синтезу застосовують хлороангідрид кислоти:
Для зв'язування утвореного хлороводню в реакційну суміш додають третинний амін (наприклад, піридин).
Іншим способом є реакція Тищенка за участі етаналю:
Взаємодія проходить у неводному середовищі при низькій температурі (0—5 °C) та у присутності каталізатору, наприклад, алкоксиду алюмінію Al(OR)3 або титану Ti(OR)4 (R — алкільний замісник).
Хімічні властивості
Етилацетат зазнає гідролізу, утворюючи оцтову кислоту і етанол. Розпад естеру пришвидшується у присутності кислот або основ:
Як типовий естер, етилацетат може реагувати із реактивами Гріньяра із утворенням третинних спиртів:
Під дією сильних відновників, таких як борогідриди або алюмогідриди лужних металів, естер відновлюється до первинного спирту:
Застосування
Етилацетат є поширеним розчинником у виготовленні покриттів, адгезивних матеріалів, чорнила, косметики, фармацевтичних препаратів. При виробництві кави без кофеїну його застосовують як екстрагент.
У харчовій промисловості використовується як добавка E1504.[2]
Див. також
Примітки
Джерела
- Шаблон:Книга Шаблон:Ref-en
- Шаблон:Книга Шаблон:Ref-en
- Шаблон:Книга Шаблон:Ref-en
- Шаблон:Книга Шаблон:Ref-en
- Шаблон:Книга