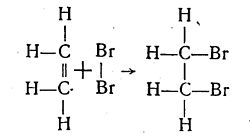Етилен
Шаблон:Перенаправлено Шаблон:Речовина Етиле́н або ете́н (IUPAC) — С2Н4, найпростіший і найважливіший представник ряду ненасичених вуглеводнів з одним подвійним зв'язком.
З 1979 року правилами IUPAC назву «етилен» рекомендовано використовувати лише для двовалентного вуглеводневого замісника –СН2–СН2–, а ненасичений вуглеводень СН2=СН2 називати «етен».
Фізичні властивості
Етилен — безбарвний газ із слабким приємним запахом. Трохи легший від повітря. У воді малорозчинний, добре розчиняється в спирті та інших органічних сполуках.
Будова
Молекулярна формула С2Н4. Структурна і електронна формули:
-
Структурна формула етилену
-
Електронна формула етилену
Хімічні властивості
На відміну від метану етилен хімічно досить активний. Для нього характерні реакції приєднання за місцем подвійного зв'язку, реакції полімеризації і реакції окиснення. При цьому один з подвійних зв'язків розривається і на його місці залишається простий одинарний зв'язок, а за рахунок звільнених валентностей відбувається приєднання інших атомів або атомних груп. Розглянемо це на прикладах деяких реакцій. При пропусканні етилену у бромну воду (водний розчин брому) остання знебарвлюється внаслідок взаємодії етилену з бромом з утворенням диброметану (бромистого етилену) C2H4Br2:
Як видно зі схеми цієї реакції, тут відбувається не заміщення атомів водню атомами галогену, як у насичених вуглеводнів, а приєднання атомів брому по місцю подвійного зв'язку. Етилен легко знебарвлює також фіолетовий колір водного розчину перманганату калію KMnO4 навіть при звичайній температурі. Сам же етилен при цьому окислюється в етиленгліколь C2H4(OH)2. Цей процес можна зобразити такими рівняннями:
Реакції взаємодії етилену з бромом і перманганатом калію служать для відкриття ненасичених вуглеводнів. Метан і інші насичені вуглеводні, як уже відзначалось, з перманганатом калію не взаємодіють.
Етилен вступає в реакцію з воднем. Так, коли суміш етилену з воднем нагріти в присутності каталізатору (порошку нікелю, платини або паладію), то вони сполучаються з утворенням етану:
Реакції, при яких відбувається приєднання водню до речовини, називаються реакціями гідрування або гідрогенізації. Реакції гідрогенізації мають велике практичне значення. їх досить часто використовують у промисловості. На відміну від метану етилен горить на повітрі світляним полум'ям, оскільки містить більше вуглецю, ніж метан. Через це не весь вуглець згоряє відразу і частинки його сильно розжарюються і світяться. Потім ці частинки вуглецю згоряють у зовнішній частині полум'я:
З повітрям етилен, як і метан, утворює вибухові суміші.
Отримання
В природі етилен не зустрічається, за винятком незначних домішок у природному газі. В лабораторних умовах етилен зазвичай одержують при дії концентрованої сульфатної кислоти на етиловий спирт при нагріванні. Цей процес можна зобразити таким сумарним рівнянням:
Під час реакції від молекули спирту віднімаються елементи води, а звільнені дві валентності насичують одна одну з утворенням подвійного зв'язку між атомами вуглецю. Для промислових цілей етилен одержують у великих кількостях з газів крекінгу нафти.
Ще один метод отримання етилену винайшли вчені національного університету Сінгапуру, за допомогою процесу штучного фотосинтезу.[1]
Застосування
В сучасній промисловості етилен застосовується досить широко для синтезу етилового спирту і виробництва важливих полімерних матеріалів (поліетилен та ін.), а також для синтезу інших органічних речовин. Дуже цікавою є властивість етилену прискорювати достигання багатьох городніх і садових плодів (помідорів, динь, груш, лимонів тощо). Використовуючи це, плоди можна транспортувати ще зеленими, а потім доводити їх до стиглого стану уже на місці споживання, вводячи в повітря складських приміщень невеликі кількості етилену.
З етилену виробляють хлористий вініл і полівінілхлорид, бутадієн і синтетичні каучуки, оксид етилену та полімери на його основі, етиленгліколь тощо.[2]
Примітки
Джерела
Посилання
Шаблон:Алкени Шаблон:Фітогормони Шаблон:Вуглеводні
- ↑ Стаття про винахід отримання етилену за допомогою штучного фотосинтезу[1] Шаблон:Webarchive
- ↑ В.П. Кухар Біоресурси – потенціальна сировина для промислового органічного синтезу Шаблон:Webarchive / Катализ и нефтехимия Сборник научных трудов. - 2007, №15.